مگنتوکموتراپی
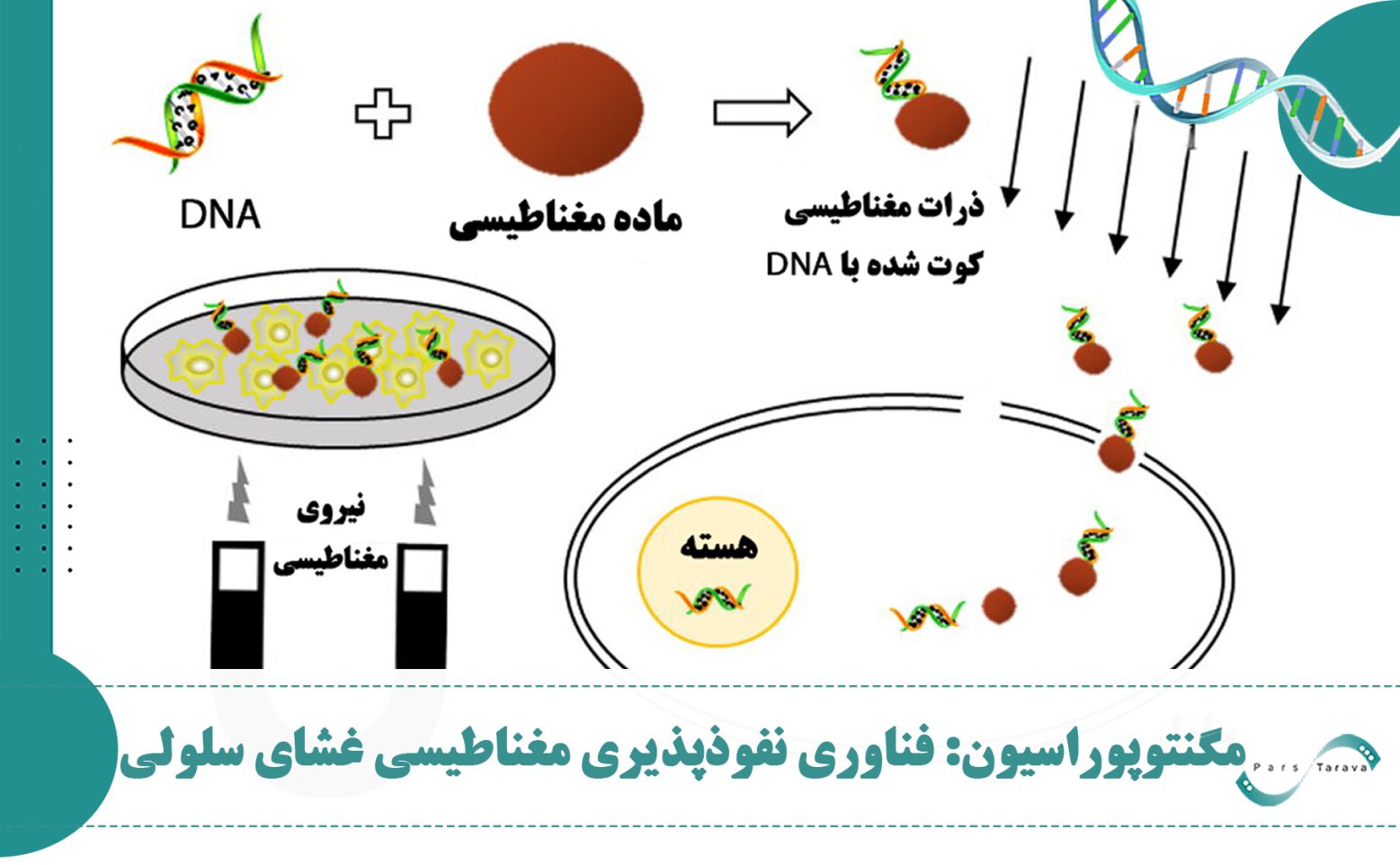
مگنتوپوراسیون: فناوری نفوذپذیری مغناطیسی غشای سلولی
مگنتوپوراسیون (Magnetoporation) یا مگنتوپوریشن یک فناوری نوین است که با استفاده از میدانهای مغناطیسی و نانوذرات، غشای سلولها را بهطور موقت نفوذپذیر میکند تا مولکولهای درمانی مانند داروها، ژنها یا پروتئینها را با کارایی بالا به درون سلولها منتقل کند. شرکت پارس تروا به عنوان شرکت پیشگام در صنعت الکتروپوریشن و الکتروکموتراپی در ایران، در این فناوری جدید نیز گوی سبقت را از سایرین ربوده و به عنوان اولین شرکت ارائه دهنده دستگاه مگنتوپوراسیون در ایران، آماده خدمت رسانی به پژوهشگران حوزه های مختلف است.
کاربرد اصلی دستگاه مگنتوپوراسیون در درمان تومورهای عمقی و مغز است. این روش بهعنوان جایگزینی امیدوارکننده برای سیستمهای سنتی تحویل مواد به سلولها مطرح شده است، زیرا دقت بالا، آسیب کم به سلولها و اثربخشی بهبودیافته را ارائه میدهد. با حرکت حوزه پزشکی به سمت درمانهای غیرتهاجمی و هدفمند، مگنتوپوریشن در خط مقدم پیشرفتهای تحویل دارو، ویرایش ژن و پزشکی بازساختی قرار دارد. این روش با اصطلاح مگنتوفکشن (magnetofection) نیز شناخته میشوند.
این فناوری بر پایه استفاده از نانوذرات مغناطیسی (MNPs) بهعنوان حامل عمل میکند. هنگامی که این نانوذرات در معرض میدان مغناطیسی متناوب قرار میگیرند، نیروهای مکانیکی ایجاد میکنند که منجر به تشکیل منافذ موقتی در غشای سلولی میشود. این منافذ، مولکولهای بزرگ را قادر میسازند تا از سد طبیعی غشا عبور کنند. مگنتوپوریشن محدودیتهای روشهای مرسوم مانند الکتروپوریشن (استفاده از پالسهای الکتریکی) و ناقلهای ویروسی (که خطرات ایمنیزایی دارند) را برطرف میکند و بهعنوان ابزاری همهکاره برای کاربردهای تحقیقاتی و بالینی شناخته میشود.
در ادامه ضمن معرفی مبانی فیزیکی و زیستی مگنتوپوراسیون، مکانیزمهای عملکرد، مزایا و محدودیتها، کاربردهای پزشکی (بهویژه در ژندرمانی و انتقال دارو)، ایمنی، پیشرفتهای تکنولوژیک و چشماندازهای آینده این فناوری بررسی میشود.
اصول مگنتوپوریشن
در روش مگنتوپوراسیون، از نانوذرات حامل مغناطیسی استفاده میشود تا تحت تأثیر میدان مغناطیسی خارجی در محل هدف تجمع یابند. نانوذرات مغناطیسی، معمولاً از جنس اکسید آهن (مانند Fe₃O₄) هستند که بهخاطر خاصیت ابرپارامغناطیسی، زیستسازگاری و امکان اصلاح سطحی گسترده انتخاب میشوند . اندازه این نانوذرات بین ۱۰ تا ۱۰۰ نانومتر است و سطح آنها با موادی مانند پلیاتیلنگلیکول (PEG) یا لیگاندهای هدفمند (مانند آنتیبادیها) پوشانده میشود تا پایداری و اتصال اختصاصی به سلولها بهبود یابد.
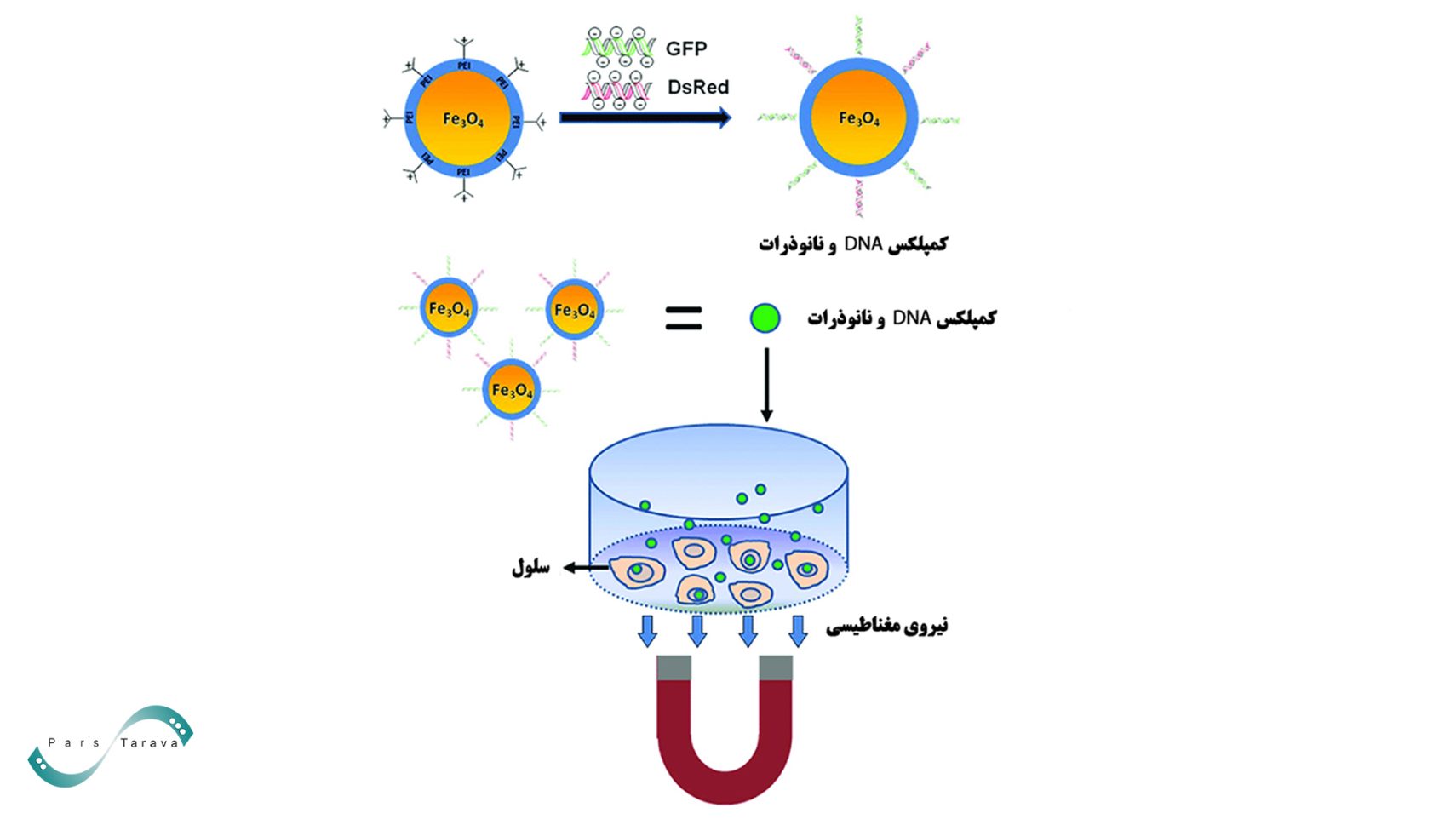
فرایند مگنتوپوریشن دو مرحله کلیدی دارد:
۱. جذب نانوذرات توسط سلول: هنگامی که این نانوذرات مغناطیسی حامل بار ژنتیکی یا دارویی به مجاورت سلولهای هدف میرسند، نیروی مغناطیسی آنها را به سطح سلولها هدایت کرده و بدین ترتیب نرخ ورود مولکولها به داخل سلول افزایش مییابد.
۲. اعمال میدان مغناطیسی: یک میدان مغناطیسی متناوب خارجی باعث ایجاد تنش مکانیکی روی نانوذرات میشود و آنها را وادار به نوسان میکند. این نیروهای مکانیکی ساختار لیپید دولایه غشا را مختل کرده و منافذ موقتی ایجاد میکنند و باعث تمایل و تمرکز نانوذرات حامل وکتورهای ژنی به سمت سلول هدف شده و انتقال سریع و مؤثر اسیدهای نوکلئیک یا داروها را فراهم میکند.
تشکیل این منافذ برگشتپذیر است و آسیب بلندمدتی به سلولها وارد نمیکند. پارامترهایی مانند قدرت میدان مغناطیسی (معمولاً ۰.۱ تا ۱۰ تسلا)، زمان اعمال میدان (از میلیثانیه تا دقیقه) و اندازه/شکل نانوذرات، تأثیر مستقیمی بر کارایی فرایند دارند . برای مثال، میدانهای قویتر تراکم منافذ را افزایش میدهند، اما نیاز به کالیبراسیون دقیق دارند تا از سمیت سلولی جلوگیری شود.
مطالعات نشان داده است که اعمال میدان مغناطیسی خارجی، در مقایسه با روشهای معمول ترانسفکشن، منجر به افزایش چشمگیر بازده انتقال ژن و نیاز به دوز کمتر ماده ژنتیکی میشود. از نظر زیستی، پس از تجمع نانوذرات در سطح سلول، فرایندهای آندوسیتوز یا سازوکارهای پمپ پروتئینی میانغشایی، باعث ورود مواد ژنتیکی یا دارویی به درون سلول میشود.
مکانیسم عملکرد مگنتوپوراسیون
مگنتوپوراسیون چند مکانیزم فیزیکی و بیولوژیکی دارد که بسته به شرایط و نوع حامل میتواند متفاوت باشد. در روشهای مبتنی بر نانوذرات مغناطیسی (مگنتوفکشن)، همانطور که اشاره شد، مولکولهای باردار (مثلاً اسید نوکلئیک) به نانوذره مغناطیسی متصل میشوند و میدان مغناطیسی خارجی باعث تراکم و متمرکز شدن این کمپلکسها در محل سلولهای هدف میشود. نیروی مغناطیسی ساختارهای حامل وکتورهای ژنی (ویروسی یا غیر ویروسی) را به سمت سلولهای هدف هدایت میکند و در نتیجه، انتقال اسیدهای نوکلئیک بسیار سریع و کارآمد میشود.
پس از رسوب نانوذرات در سطح سلول، ذرات فلزی میتوانند بر غشاء سلولی اثرات موضعی مکانیکی یا میدان الکترومغناطیسی کوچک ایجاد کرده و نفوذپذیری غشاء را افزایش دهند. همچنین ذرات مغناطیسی پوششدار با حاملهای کاتیونی میتوانند از طریق فرآیند اندوسیتوز به راحتی وارد واکوئلهای داخلسلولی (اندوزوم) شوند و سپس محتویات خود را آزاد کنند.
در روش مگنتوپوراسیون دارویی (برای انتقال داروهای شیمیدرمانی)، معمولاً میدان مغناطیسی پالسی قوی به تومور یا سلولهای بیمار اعمال میشود تا پس از تزریق دارو (مانند بلئومایسین)، نفوذپذیری غشاء سلولی افزایش یابد. برای نمونه در یک مطالعه روی موشهای توموری، پالسهای مغناطیسی (بزرگی ۳.۵ تسلا، ۸ پالس ۱۶۰ میکروثانیهای در ۱ هرتز) بهصورت غیرتهاجمی پس از تزریق اینتراتومورال بلئومایسین اعمال شد و مشاهده گردید که میزان داروی نفوذیافته به سلولهای سرطانی در گروه میدان مغناطیسی حدود ۷ برابر بیشتر از گروه کنترل بود.
این نتایج نشان میدهد که اعمال پالس مغناطیسی میتواند نفوذپذیری غشای سلولی را افزایش دهد، هرچند دستیابی به نفوذپذیری معنادار نیازمند میدان قویتر یا زمان تابش طولانیتر است.
مزایای مگنتوپوراسیون
مگنتوپوراسیون مزایای متعددی نسبت به روشهای سنتی انتقال ژن یا دارو دارد. از جمله این مزایا میتوان به افزایش بازده انتقال، کاهش دوز مورد نیاز ماده ژنتیکی، و روند سریعتر تحویل اشاره کرد.
هدفمندی و ایمنی بالا
در مقایسه با ترانسفکشن کلاسیک با لیپوزوم یا پلیمرهای کاتیونی، مگنتوفکشن به کمک تراکم میدان مغناطیسی میتواند در نواحی محدود و تعیینشده (مثلاً روی سلولهای یک تومور) ژنها را منتقل کند، که همین موضوع باعث تمرکز بالا و کاهش اثرات جانبی سیستمیک میشود. نانوذرات اصلاحشده، اثرات خارج از هدف را کاهش میدهند و نسبت به ناقلهای ویروسی که ممکن است بهصورت تصادفی در ژنوم ادغام شوند، ایمنتر هستند.
آسیب کمتر به سلولها
علاوه بر این، فناوری مگنتوپوراسیون نسبتاً غیرتهاجمی است؛ برای مثال برخلاف الکتروپوراسیون که نیاز به الکترود درونزا دارد، این روش بدون تماس مستقیم با بافت عمل کرده و از احتمال تحریک عضلانی یا عوارض الکتریکی کاهش مییابد.
مقیاسپذیری
این روش برای کاربردهای گسترده، از دستکاری تکسلولی تا درمان در سطح اندامها مناسب است.
چالشها و محدودیتهای مگنتوپوراسیون
با وجود مزایای بسیار این روش، محدودیتهایی نیز برای مگنتوپوراسیون وجود دارد.
- برای هدایت مؤثر نانوذرات، باید میدان مغناطیسی نسبتاً قوی و با گرادیان بالا فراهم شود؛ لذا در عمقهای زیاد بدن یا بافتهای ضخیم این روش دشوار است. علاوه بر این، رساندن نانوذرات مغناطیسی به محل هدف (مثلاً تومور بزرگ) ممکن است نیازمند تزریق موضعی یا طراحی خاص حامل باشد. همچنین تنوع در روشهای سنتز نانوذرات و پارامترهای میدان مغناطیسی، بازتولیدپذیری نتایج را دشوار میکند.
- برخی پوششهای پلیمری مانند PEI سمی هستند و مقدار زیاد استفاده از آنها میتواند سمیت سلولی ایجاد کند، هرچند در روشهای مگنتوفکشن معمولاً از مقادیر کاهشیافته PEI استفاده میشود تا تعادل بین کارایی و سمیت حفظ شود. در مطالعه ذکر شده نیز مشخص گردید که برای دستیابی به بیان ژنی قابلتوجه، تنظیم دقیق pH و ترکیب پوشش نانوذره ضروری است، که پیچیدگی تولید حاملها را افزایش میدهد.
کاربردهای مگنتوپوراسیون
مگنتوپوراسیون در زمینههای مختلفی بهویژه در دو زمینه مهم پزشکی زیر کاربرد دارد:
ژن درمانی:
در ژندرمانی، انتقال مؤثر سیستمهای ویرایش ژن مانند CRISPR-Cas9 یا siRNA بهدلیل اندازه و بار الکتریکی آنها چالشبرانگیز است. مگنتوپوریشن با کارایی انتقال تا ۸۰٪ در سلولهای اولیه، از الکتروپوریشن پیشی میگیرد و به کمک نانوذرات مغناطیسی این امکان را فراهم میکند که ژن با دقت بالا به سلولهای هدف برسد. بررسیها نشان دادهاند که انواع مختلف ژن را میتوان با این روش به بافتهای سلولی منتقل کرد و در مدلهای حیوانی، بیان ژنهای هدف (مثلاً ژن تومور سرکوبگر یا آنزیم پروموتر) بهخوبی انجام شده است. بهعنوان مثال، میتوان از وکتورهای ویروسی (آدنوویروس و AAV) و یا غیر ویروسی (لیپوزومها و پلیمرها) بهره برد که با اتصال به نانوذرات مغناطیسی، در حضور میدان مغناطیسی به سرعت وارد سلول میشوند.
تحویل هدفمند داروها:
مگنتوپوریشن امکان انتقال داروهای شیمیدرمانی را مستقیماً به سلولهای تومور فراهم میکند و سمیت سیستمیک را کاهش میدهد. مطالعات، نشان میدهد که جذب دوکسوروبیسین در سلولهای سرطانی با این روش ۶۰٪ نسبت به انتشار غیرفعال افزایش یافته و آپوپتوز (مرگ برنامهریزیشده سلولی) را بهطور چشمگیری تقویت میکند. مطالعات متعددی تأیید کردهاند که مگنتوفکشن در هر دو مدل آزمایشگاهی و پیشبالینی بازده بالایی دارد و در برخی موارد باعث نفوذپذیری بالای سلولهای توموری به عوامل ژن درمانی شده است. این روش در اصل شبیه الکتروپوراسیون است اما به صورت کاملاً تماسناپذیر اجرا میشود و میتواند به کاهش نیاز به دوزهای بالای شیمیدرمانی و در نتیجه کاهش عوارض منجر گردد. علاوه بر این، مگنتوپوراسیون با استفاده از نانوذرات مغناطیسی نیز در مطالعات ترکیبی (مانند مگنتوشیمیدرمانی) بررسی شده است تا تمرکز داروی ضدسرطان در محل تومور افزایش یابد. بدین ترتیب، چشمانداز اصلی آن بهبود اثر درمانی و کاهش سمیت سیستمیک است.
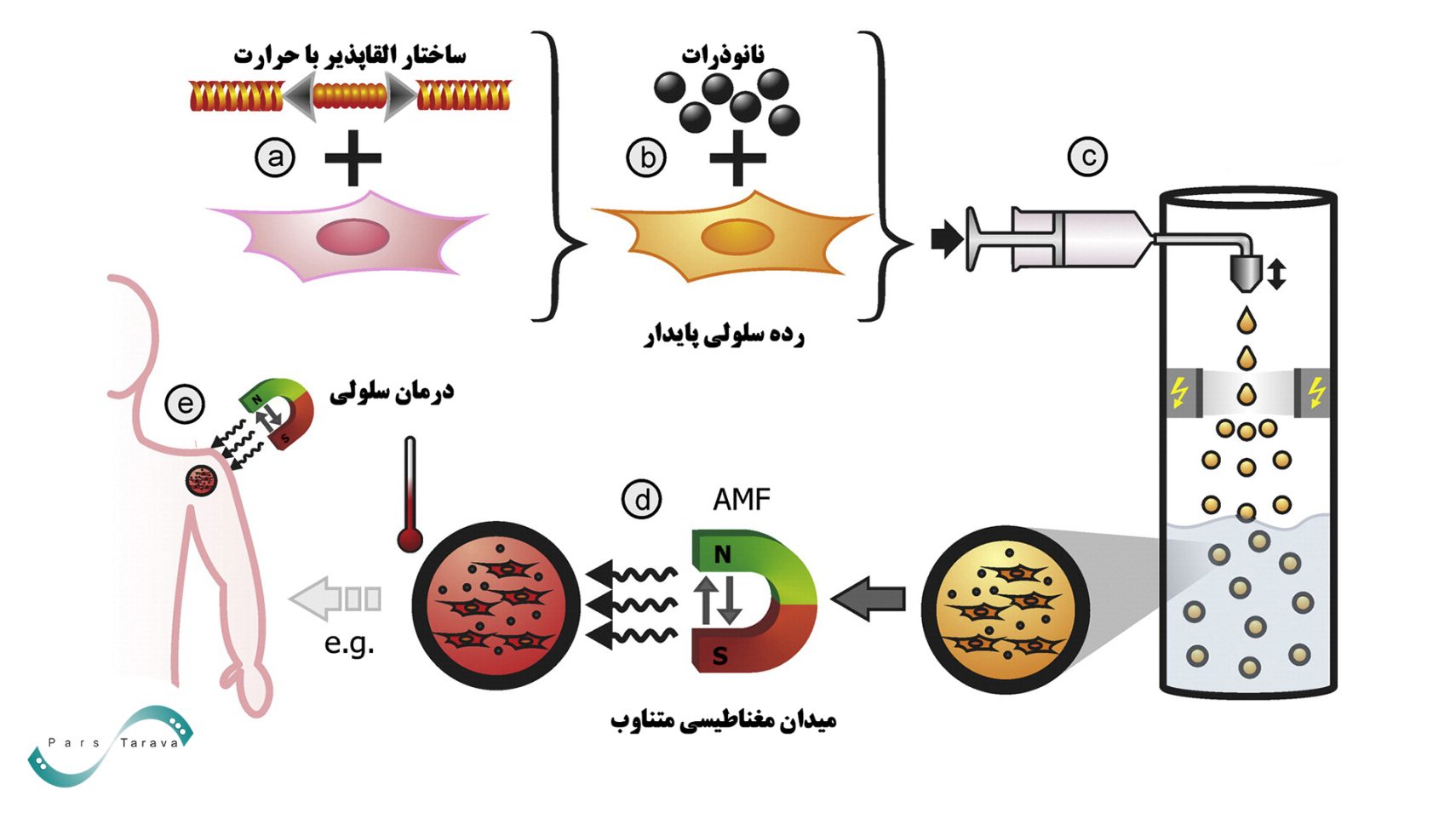
درمان سرطان با هایپرترمی مغناطیسی:
نانوذرات مغناطیسی بارگذاریشده با عوامل حساس به دما میتوانند با فعالشدن توسط میدان مغناطیسی، گرمای موضعی تولید کنند. در مطالعهای، میدان مغناطیسی متناوب باعث ازبینرفتن ۷۰٪ سلولهای گلیوبلاستوما در شرایط آزمایشگاهی شد، در حالی که بافتهای سالم آسیبی ندیدند.
پزشکی بازساختی:
مگنتوپوریشن انتقال فاکتورهای رشد یا mRNA به سلولهای بنیادی را تسهیل میکند. در مطالعهای مرتبط با بازسازی غضروف، نانوذرات مغناطیسی mRNA رمزکننده پروتئین BMP-2 را به سلولهای بنیادی مزانشیمی رساندند و منجر به ۳ برابر شدن تمایز غضروفی نسبت به روشهای مرسوم شدند.
ایمنی روش مگنتوپوراسیون
از نظر ایمنی، مگنتوپوراسیون یکی از مزایای بالقوه خود را در غیرتهاجمی بودن آن نشان میدهد؛ بدون نیاز به الکترود یا تماس قوی با بافت، احتمال ایجاد سوختگی یا صدمات فیزیکی کاهش مییابد. نانوذرات اکسید آهن فوقپارامغناطیسی غالباً سازگار با بیوفیزیولوژی بدن محسوب میشوند (همچون کاربردشان در تصویربرداری MRI) و در اثر فرآیندهای طبیعی تخریب میشوند، اما نیاز به بررسی سمیت پوششها (مثل پلیمرهای کاتیونی) و تجمع احتمالی آنها در ارگانها وجود دارد. همچنین پالسهای قوی مغناطیسی میتوانند در صورت استفاده نامناسب، موجب گرمایش یا آسیب مکانیکی به بافت شوند؛ لذا ارزیابی دقیق پارامترهای میدان و زمان تابش برای اطمینان از ایمنی ضروری است. مطالعات اولیه نشان میدهد که اثرات جانبی مگنتوپوراسیون نسبتاً اندک است، اما انجام تحقیقات جامعتر در مدلهای حیوانی و بالینی برای بررسی سمیت درازمدت و پاسخ ایمنی ضرورت دارد.
پیشرفتهای فناوری مرتبط با مگنتوپوراسیون
تحقیقات پیشرفته روی مگنتوپوراسیون شامل طراحی انواع جدیدی از نانوذرات مغناطیسی و بهینهسازی میدانهای مغناطیسی کاربردی است. بهعنوان نمونه، روشهای سنتز نانوذرات اکسید آهن به گونهای تکامل یافتهاند که با پوششهای چند لایه و ترکیب با لیگاندهای ویژه، بازده انتقال و ثبات شیمیایی را افزایش میدهند. نانوذرات هوشمند پاسخگو به محرکهایی مانند pH یا دما، امکان رهایش کنترلشده محموله را فراهم میکنند. بهعنوان مثال، نانوذرات حساس به pH، داروها را فقط در محیط اسیدی تومورها رها میکنند. نانوذرات ساختهشده از آلیاژهای منیزیم که پس از انتقال مواد تجزیه میشوند نیز خطر تجمع در بدن را از بین میبرند .
علاوه بر این، ترکیب فناوری مگنتوپوراسیون با روشهای دیگر نیز در حال بررسی است؛ مانند کاربرد میدانهای مغناطیسی پالسی نوسان گر متناوب بهمنظور ایجاد برهمکنشهای مکانیکی مؤثرتر با غشاء سلولی. ترکیب مگنتوپوریشن با الکتروپوریشن (مگنتو-الکتروپوریشن) نیز کارایی انتقال را در سلولهای عصبی تا ۴۰٪ افزایش داده است. مطالعات اولیه از قبیل استفاده از کربن نانولولهها نشان دادهاند که میتوان با میدان مغناطیسی ضعیف، اثر قابلتوجهی روی غشاء سلولهای سرطانی داشت.
بهعلاوه، تلاشهایی در زمینه استفاده از مولکولهای حساس به میدان مغناطیسی (مانند فریتین مهندسیشده) برای کنترل ژنهای درونسلولی با اعمال میدان مغناطیسی (مگنتوژنتیک) وجود دارد که میتواند افقهای جدیدی در ژندرمانی گشوده کند.
چشمانداز آینده
در آینده، پیشرفتهای بیشتر در این حوزه بر بهبود مواد حامل و افزایش ایمنی متمرکز خواهد بود. بهعنوان مثال، نانوذرات مغناطیسی با پوششهای زیستسازگار جدید (پپتیدی یا پلیمرهای طبیعی) میتوانند سمیت را کاهش داده و کارایی را افزایش دهند. همچنین، توسعه ژنها و داروهای جدید سازگار با انتقال مغناطیسی و ارزیابی ترکیب مگنتوپوراسیون با فناوریهای موازی (مانند میکروپلاسمای مغناطیسی و بیوراکتورهای مخصوص) ادامه خواهد یافت.
از سوی دیگر، لازم است مطالعات بالینی بیشتری برای اثبات کارایی و ایمنی این روش در انسان انجام شود. با فراهم آمدن میدانهای مغناطیسی قویتر (مانند MRI پیشرفته یا آهنرباهای ابررسانا) و نانوذرات هوشمندتر، انتظار میرود مگنتوپوراسیون نقش بارزی در ژندرمانی آینده و دارورسانی هدفمند داشته باشد.
در مجموع، مگنتوپوراسیون فناوری نوینی است که ترکیب نانوذرات مغناطیسی با میدان مغناطیسی را برای افزایش نفوذپذیری غشای سلولی به کار میگیرد. شرکت پارس تراوا اولین تولید کننده دستگاه مگنتوپوریشن در ایران است و همواره تلاش می کند همگام با فناوری روز دنیا، تولیدات خود را گسترش دهد. تحقیقات انجامشده نشان داده است که این روش میتواند بازده انتقال ژن و دارو را بهطور قابلتوجهی افزایش دهد و با برطرف کردن برخی محدودیتهای روشهای سنتی، چشماندازهای جدیدی در درمانهای ژنتیکی و دارویی ایجاد کند.
منابع:
Magnetoporation: New Method for Permeabilization of Cancerous Cells to Hydrophilic Drugs
Magnetofection: A Reproducible Method for Gene Delivery to Melanoma Cells
Magnetically enhanced nucleic acid delivery. Ten years of magnetofection—Progress and prospects







